Infecção COVID-19 no ciclo gravídico-puerperal
CORONAVIRUS
São Paulo, 08 de julho de 2020
Infecção COVID-19 no ciclo gravídico-puerperal
Silvana Maria Quintana
Professora-associada livre-docente do Departamento de Ginecologia e Obstetrícia da Faculdade de Medicina de Ribeirão Preto da Universidade de São Paulo
Geraldo Duarte
Professor Titular do Departamento de Ginecologia e Obstetrícia da Faculdade de Medicina de Ribeirão Preto da Universidade de São Paulo
Desde a notícia sobre casos de pneumonia de causa desconhecida na província de Hubei, na República Popular da China, no final de 2019, o mundo tem assistido apreensivo à evolução de uma das maiores pandemias da história da humanidade. A identificação de um novo tipo de coronavírus, nunca isolado previamente em humanos, denominado Severe Acute Respiratory Syndrome-Related Coronavirus 2 (SARS-CoV-2) como agente etiológico da Coronavirus Disease 2019 (COVID-19)1,2 e a rápida disseminação dessa infecção viral por diversos continentes fez com que a Organização Mundial da Saúde (OMS)3 declarasse estado de pandemia em 11 de março de 2020. Desde então, observou-se rápido e crescente aumento do número de casos de COVID-19, com consequente aumento do número de óbitos, e medidas não farmacológicas e farmacológicas têm sido propostas para o enfrentamento da pandemia. Inicialmente foram utilizadas informações sobre o comportamento de outros agentes virais causadores de infecções, como o vírus H1N1 e outros dois coronavírus, o SARS-CoV (China) e o MERS-CoV (Oriente Médio), entretanto a COVID-19 tem mostrado características distintas. Destaca-se que, pelo fato de ser uma infecção recente, o conhecimento da COVID-19 está em construção, sendo necessária atualização diária sobre esse assunto.
Com quem estamos lidando?
O SARS-CoV-2 é um RNA vírus pertencente à família Coronaviridae do gênero Betacoronavirus. Por ser um RNA vírus, apresenta maior tendência de mutações e sua fácil disseminação frequentemente causa picos epidêmicos. Segundo informações do Centro de Controle e Prevenção de Doenças (CDC) da China, o SARS-CoV-2 é o resultado de recombinações virais, que lhe permitiram escapar do ciclo animal-animal, passando a infectar seres humanos. Isso o caracteriza como uma zoonose, que, hipoteticamente, tem o morcego como hospedeiro primário1.
Curso da infecção COVID-19
Período de incubação do SARS-CoV-2: Vai desde a contaminação do indivíduo até o aparecimento dos sinais e sintomas. Dura, em média, 5 dias, variando entre 2 dias e 14 dias4.
Transmissão viral: Ocorre por meio de secreções respiratórias expelidas por tosse ou espirro, contato pessoal próximo com pessoas infectadas e fômites contaminados com o vírus depositados em superfícies3-5.
Quadro clínico: De acordo com o CDC americano6, cerca de 30% dos pacientes com COVID-19 são assintomáticos. Dentre os sintomáticos, 20% podem necessitar atendimento hospitalar em decorrência de dificuldade respiratória e aproximadamente 5% podem necessitar de suporte ventilatório para o tratamento de insuficiência respiratória. Esses porcentuais têm se mantido na população de gestantes. De acordo com o Boletim Epidemiológico Especial do Ministério da Saúde do Brasil referente à semana epidemiológica 21 (17 a 23 de maio de 2020)7, que incluiu dados sobre gestantes e puérperas, a tosse foi o sintoma mais frequente (80,6%), seguida por febre (73%) e dispneia (62%). O sinal clínico mais frequentemente associado a óbito materno foi a queda da saturação de oxigênio abaixo de 95%. Aproximadamente 90% dos pacientes apresentam mais de um sintoma5. As principais manifestações clínicas estão apresentadas no Quadro 1.
Quadro 1: Principais manifestações clínicas da infecção COVID-19.
|
Assintomáticos |
30% a 80% |
| Sintomáticos | 20% a 70% |
|
Sintomas mais comuns: - Febre (> 37,8ºC) - Tosse - Dispneia - Mialgia - Fadiga |
Sintomas menos comuns: - Anorexia, náusea/vômito - Dor de garganta - Produção de escarro - Dor de cabeça - Confusão mental - Tonturas - Dor no peito - Hemoptise - Dor abdominal - Diarreia - Congestão conjuntival - Anosmia súbita ou hiposmia |
| Cerca de 5% dos pacientes apresentarão sinais de baixa oxigenação por insuficiência respiratória e choque. |
Transmissibilidade do SARS-CoV-2 de acordo com o quadro clínico:
Questionamentos têm sido levantados sobre a eficácia da transmissão do SARS-CoV-2. Na Figura 1, observa-se o porcentual de transmissibilidade de acordo com a fase da infecção.
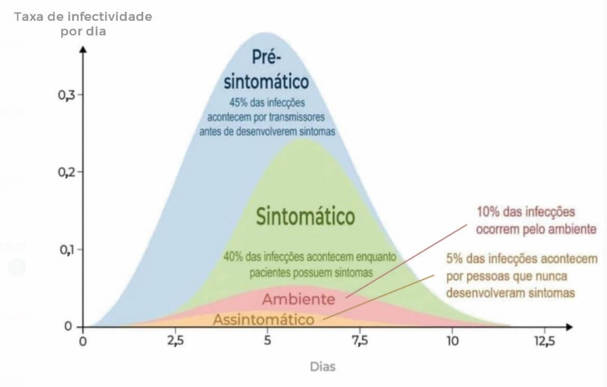
Figura 1: Transmissibilidade do SARS-CoV-2 de acordo com a fase da infecção. (Adaptado de Ferretti et al., 20208.)
De acordo com o Ministério da Saúde9 e com a Secretaria de Estado da Saúde de São Paulo10, para definição de caso grave pelo menos uma das alterações citadas a seguir deve estar presente:
– Frequência respiratória > 25 incursões respiratórias por minuto (irpm);
– Saturação de oxigênio < 95%;
– Sem melhora da saturação, apesar da oferta de oxigênio;
– Hipotensão arterial;
– Alteração do tempo de enchimento capilar;
– Alteração do nível de consciência;
– Oligúria.
Diagnóstico laboratorial da infecção pelo SARS-CoV-211-14: Pode ser realizado por diferentes testes, descritos a seguir:
– Testes relacionados à detecção de partículas virais: reação em cadeia da polimerase (RT-PCR), teste rápido molecular para identificação de genes, e testes de identificação de antígenos virais;
– Testes para identificação de anticorpos contra o SARS-CoV-2: quantificam IgA, IgM e IgG utilizando diferentes técnicas; e
– Testes rápidos para identificação de anticorpos ou antígenos virais.
O RT-PCR (qRT-PCR) é considerado padrão de referência para a identificação do SARS-CoV-2 e se baseia na detecção de sequências únicas de RNA viral. É realizado em amostras biológicas, sendo a coleta de amostras da cavidade nasal e da orofaringe a mais utilizada. Nas áreas em que a COVID-19 está amplamente disseminada, um ou mais resultados negativos de um caso suspeito não descartam a possibilidade de infecção viral, particularmente quando foram analisadas apenas amostras do trato respiratório superior. Nesses casos, pode-se indicar a coleta de amostras de vias respiratórias inferiores e testar novamente. Entre os fatores que elevam a probabilidade de resultado negativo em um indivíduo infectado destacam-se: má qualidade da amostra, contendo pouco material do paciente; amostra coletada em fase muito precoce ou tardia da infecção (a coleta ideal é a realizada entre o terceiro e o sétimo dias do início dos sintomas); amostra inadequadamente manuseada e enviada; e razões técnicas inerentes ao teste, como mutação do vírus ou inibição da PCR.
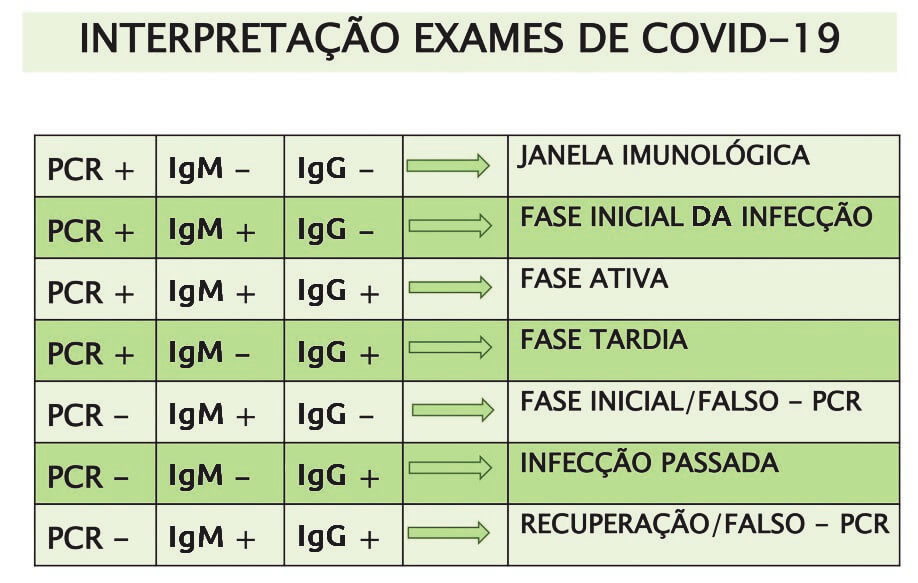
Os testes sorológicos detectam a presença de anticorpos específicos ou de pool de anticorpos em amostra sanguínea. Devem ser realizados somente após o sétimo dia do início dos sintomas. Podem ser utilizados para checar a soroprevalência populacional.
A Figura 2 ilustra a linha do tempo para a infecção COVID-19 de acordo com os testes diagnósticos e sua respectiva interpretação.
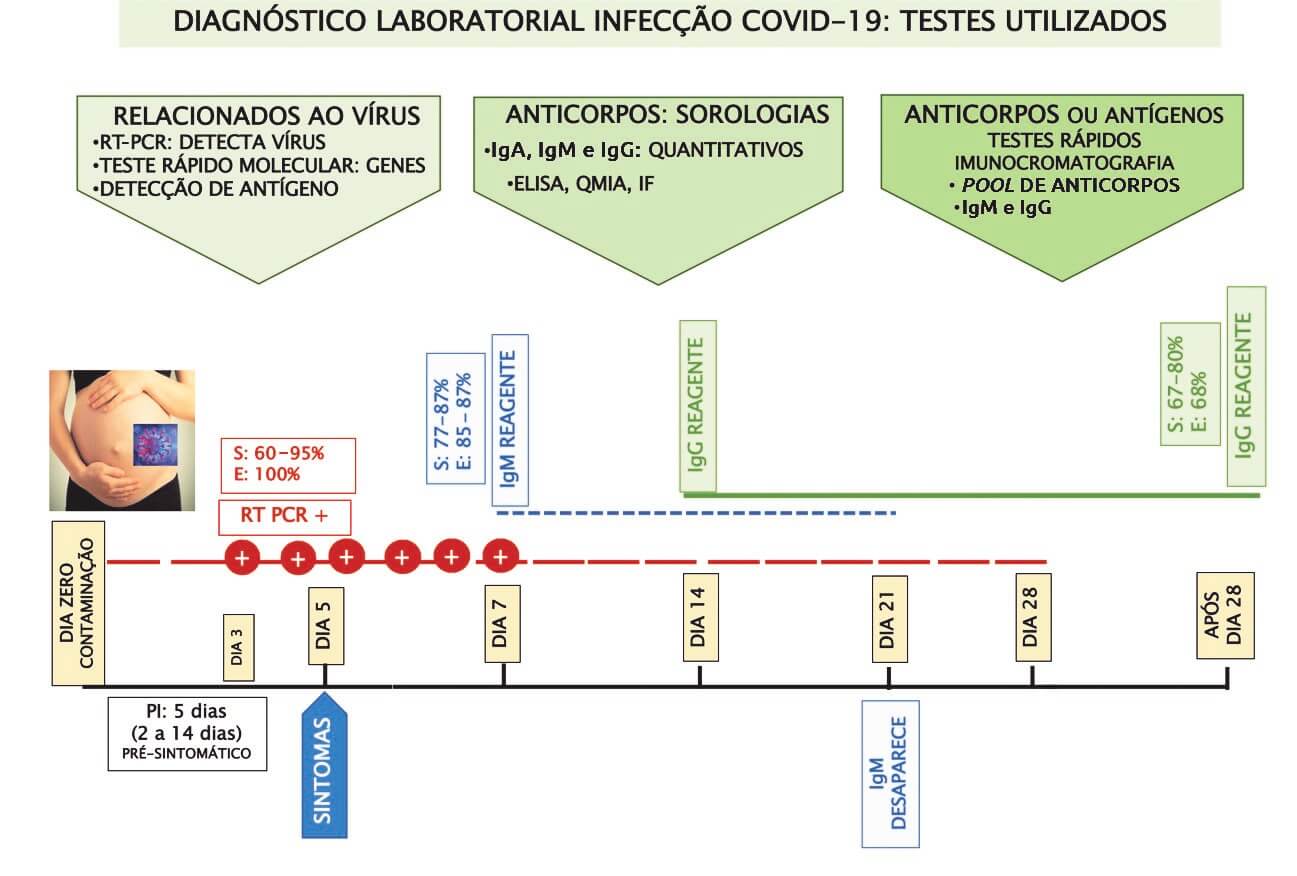
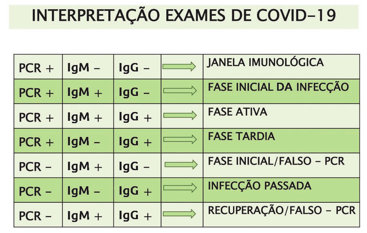
E = especificidade; S = sensibilidade; PI = período de incubação
Figura 2: Linha do tempo para a infecção COVID 19 de acordo com os testes diagnósticos e sua respectiva interpretação. (Adaptado de Tang et al., 202015; Chen et al., 202016.)
Após 6 meses de evolução da pandemia, muito já se conhece sobre os efeitos do SARS-CoV-2 no organismo humano. A evolução da infecção pode ser dividida em três estágios de acordo com a gravidade da doença, caracterizada pelos quadros clínico e laboratorial do paciente. Na Figura 3 observam-se os três estágios da infecção, as características clínicas e laboratoriais, assim como os possíveis tratamentos para a COVID-19.
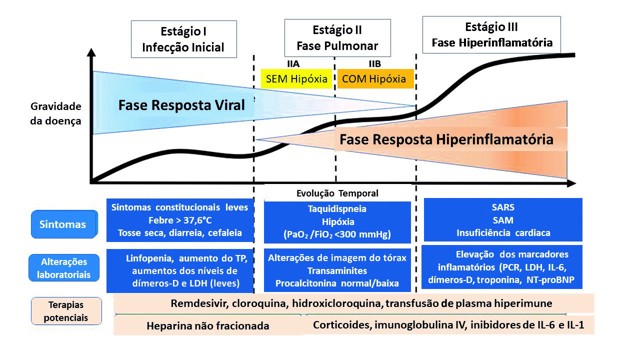
FiO2 = fração inspirada de oxigênio; IL = interleucina; LDH = desidrogenase láctica; NT-proBNP = porção N-terminal do pró-hormônio do peptídeo natriurético do tipo B; PaO2 = pressão parcial de oxigênio no sangue arterial; PCR = proteína C-reativa; SAM = síndrome de ativação macrofágica; SARS = síndrome respiratória aguda grave; TP = tempo de protrombina.
Figura 3: Estágios da COVID-19, quadros clínico e laboratorial, e potenciais terapêuticas. (Adaptado de Siddiqi e Mehra, 202017.)
Manejo de gestantes e puérperas com suspeita/diagnóstico de COVID-19
Com o significativo aumento do número de casos de COVID-19 cresceu a preocupação com a ocorrência dessa infecção durante o ciclo gravídico-puerperal. As importantes adaptações do organismo feminino à gravidez, com destaque à modulação do sistema imunológico, bem como a experiência prévia com a gravidade da infecção pelo H1N1 nesse grupo de mulheres mobilizaram os serviços de atenção às mulheres para o cuidado no ciclo gravídico-puerperal em todo o mundo. Embora os dados da literatura não apontem maior predisposição para aquisição da COVID-19 por gestantes e puérperas, por analogia de que pacientes com comorbidades apresentam maior risco de adquirir essa infecção viral e ter evolução desfavorável, é natural o raciocínio de que gestantes de alto risco por doenças como hipertensão e diabetes também possam apresentar pior evolução da COVID-19. A revisão da literatura aponta que as gestantes têm quadro clínico semelhante ao de não gestantes, a maioria delas apresenta quadros clínicos leves a moderados, e 1% a 5% necessitarão de suporte ventilatório e/ou cuidados em Unidade de Terapia Intensiva (UTI). No Brasil, segundo orientações do Ministério da Saúde, gestantes e puérperas até o 14o dia de pós-parto devem ser consideradas grupo de risco para COVID-193.
Ainda de acordo com o Boletim Epidemiológico Especial do Ministério da Saúde do Brasil referente à semana epidemiológica 217, que incluiu dados sobre gestantes e puérperas, 1% dos casos de síndrome respiratória aguda grave (SRAG) causada por SARS-CoV-2 ocorreu em gestantes, das quais 58,3% foram internadas na UTI e 72,2% fizeram uso de suporte ventilatório, sendo 80,8% do tipo invasivo. Destaca-se que 53% desses casos ocorreram na Região Sudeste. Nesse período, foram confirmados 36 óbitos por COVID-19 em gestantes ou puérperas com SRAG, 55,5% dos quais na Região Sudeste.
A literatura disponível aponta que, em relação aos desfechos maternos e perinatais, a infecção pelo SARS-CoV-2 agrega elevada taxa de cesárea (70%), e as taxas de prematuridade podem chegar a 47%, de morte fetal a 2,1%, e de morte perinatal a 7,1%18-21. A transmissão vertical tem sido descrita em relatos de caso, apontando que é possível, mas parece ter baixo potencial de transmissão da mãe para o filho.
Com o intuito de guiar ginecologistas e obstetras na atenção às mulheres no ciclo gravídico-puerperal durante a pandemia COVID-19, diferentes sociedades médicas e instituições profissionais internacionais, entre elas American College of Obstetricians and Gynecologists (ACOG)22, Royal College of Obstetricians and Gynecologists (RCOG)23 e Federação Internacional de Ginecologistas e Obstetras (FIGO)24, além de sociedades nacionais, como SOGESP25 e Associação de Ginecologistas e Obstetras de Minas Gerais (SOGIMIG)26, publicaram diretrizes para o atendimento de pacientes grávidas, abrangendo triagem pré-natal, atendimento pré-parto, cuidados intraparto durante diferentes estágios do trabalho de parto em situações de emergência e não emergenciais, bem como cuidados e acompanhamento pós-parto. Destaca-se que cada serviço de saúde deve adaptar as diretrizes a sua realidade. A seguir um resumo das recomendações das diversas diretrizes27:
Cuidados na atenção pré-natal
a) Todos os serviços de saúde devem organizar uma triagem para gestantes, considerando sintomas e exposição. Acrescenta-se que essa triagem deve ser realizada também em acompanhantes.
b) O uso da telemedicina é incentivado para as consultas pré-natais (em especial para gestações de baixo risco), possibilitando a organização de consultas presenciais, exames laboratoriais e ultrassonografia.
c) Exames laboratoriais e ultrassonografia devem ser agendados, se possível, no mesmo dia da consulta pré-natal.
d) Todo o equipamento de ultrassom e as salas de atendimento devem ser limpos adequadamente após cada uso.
e) Recomendar o uso de máscara de tecido às gestantes assintomáticas.
f) Recomendar vacinas, especialmente vacina contra H1N1.
g) Manejo de gestantes sintomáticas ou com diagnóstico de COVID-1928,29 (Figura 3):
– Gestantes classificadas no Estágio I: recomendam-se apenas medidas de suporte, que consistem em repouso, hidratação, analgésicos e antitérmicos com monitorização da evolução dos sintomas. Essas gestantes serão mantidas em isolamento domiciliar, sendo importante o contato telefônico realizado pela equipe de saúde (duas a três vezes por semana) e o fornecimento de orientações escritas sobre sinais de gravidade e quando e onde procurar o serviço de saúde. A SOGESP elaborou um folder para orientação das gestantes, que pode ser acessado no site https://www.sogesp.com.br/noticias/coronavirus/?page=5&&&.
– Gestantes classificadas no Estágio II: necessitam internação, pois apresentam febre, taquipneia/dispneia ou sinais de acometimento de vias aéreas inferiores, com sinal radiográfico de pneumonia. Nesse estágio, várias medicações têm sido propostas, mas cada serviço deve estabelecer um protocolo de tratamento. Dentre as medicações que podem ser usadas nesse estágio estão:
- Antibióticos: azitromicina, amoxacilina com clavulanato ou ceftriaxona.
- Heparina sódica: usar somente em caso de contagem plaquetária > 50.000/mm³, sem sangramento e com baixo risco de sangramento. Se a contagem estiver entre 30 mil e 50 mil plaquetas, discutir com o hematologista. Seguir o esquema de doses apresentado no Quadro 2. Também pode ser utilizada enoxaparina (baixo peso molecular) na dose de 40-60 mg/dia por via subcutânea.
Quadro 2: Esquema de doses, de acordo com o peso da paciente.
| Peso | Até 60kg | 60 kg a 90 kg | > 90 kg |
| Heparina |
5.000 UI 12/12 horas |
5.000 UI 8/8 horas |
7.500 UI 8/8 horas |
- Corticoide: considerar após 7 dias do início dos sintomas em caso de necessidade de suplementação de oxigênio > 4 l/min ou aumento de 20% da necessidade de oxigênio suplementar em 24 horas. A escolha é a metilprednisolona na dose de 40 mg 12/12 horas por 3 dias a 7 dias.
- Oseltamivir até obter resultado do RT PCR para SARS-CoV-2.
– Gestantes classificadas no Estágio III: esse estágio caracteriza-se por um estado de “hiperinflamação” e/ou suspeita de síndrome de ativação macrofágica, em especial os casos com febre persistente, grave acometimento pulmonar (> 50% em área na tomografia computadorizada), duas citopenias, hipertrigliceridemia, e ferritina > 2.000 ng/ml. Recomenda-se:
- Manter as drogas prescritas no Estágio II.
- Solicitar anticorpos antifosfolípides (anticorpos anticardiolipina – ACA, anti-β2-glicoproteína I e pesquisa de inibidor lúpico – PIL).
- Solicitar exames para avaliar síndrome de ativação macrofágica (SAM). Neste caso, recomenda-se o uso de dexametasona na dose de 8-16mg dia por via endovenosa.
No Estágio III, a gestante/puérpera deverá estar na UTI sob assistência multidisciplinar, pois haverá necessidade de outras intervenções e de novos medicamentos de acordo com os diferentes protocolos dos serviços de saúde. Nesse estágio, a equipe deverá monitorizar a vitalidade fetal e a resolução da gravidez deve fazer parte da discussão interdisciplinar.
A pronação de pacientes nesse estágio tem mostrado ser medida valiosa no manejo dessa fase da infecção; entretanto, a depender da idade gestacional, esse posicionamento pode requerer uma adaptação do leito.
Essas condutas estão, em parte, organizadas no algoritmo apresentado na Figura 4.
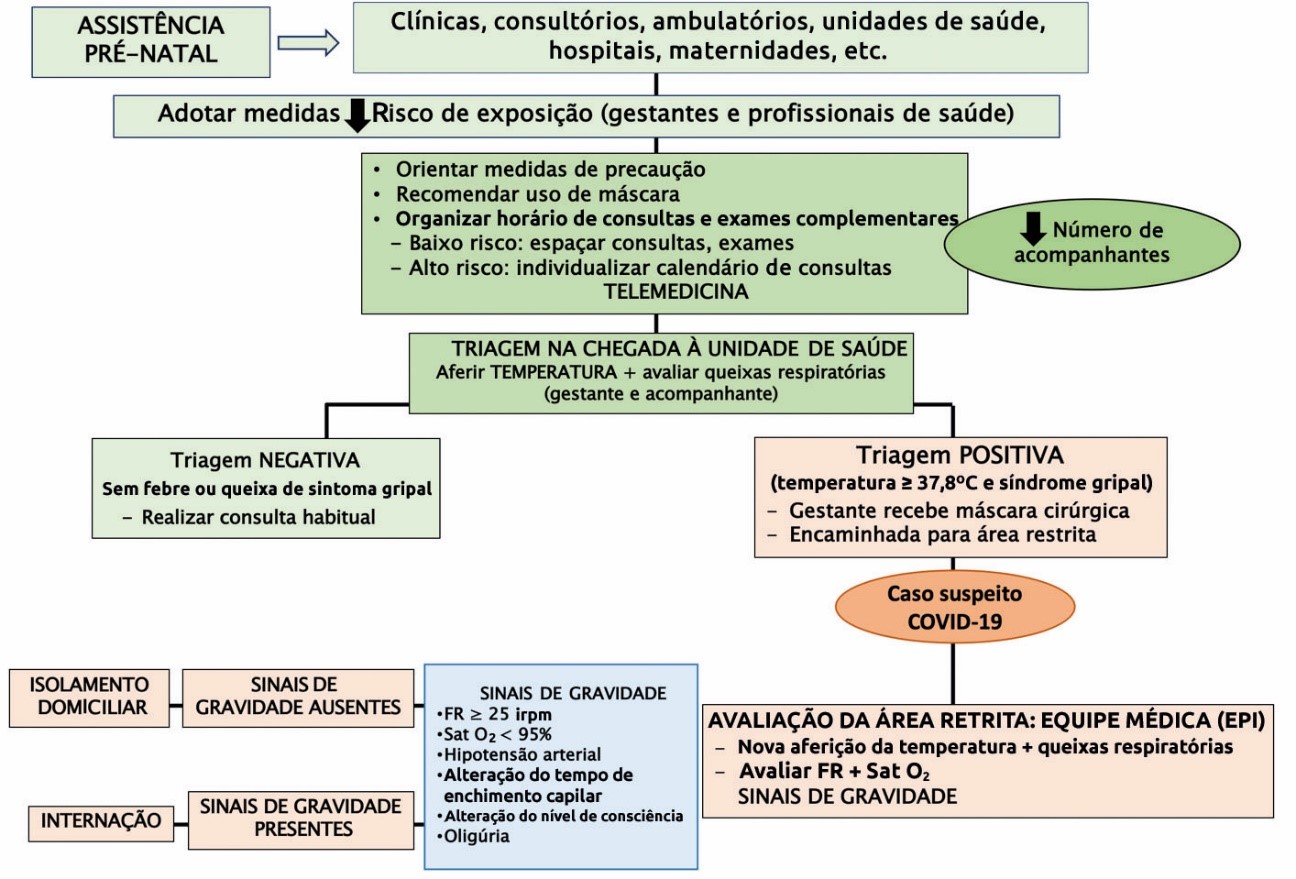
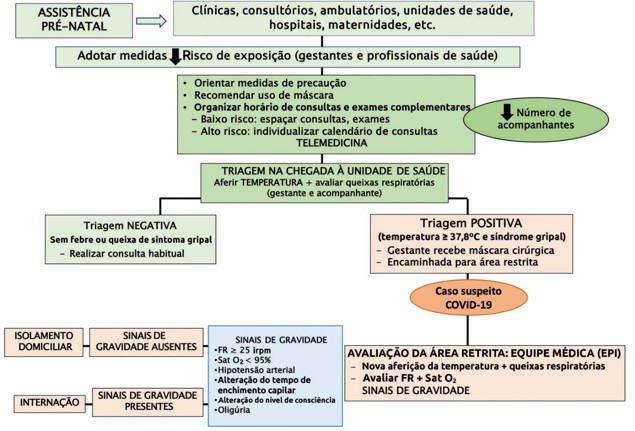
EPI = equipamento de proteção individual; FR = frequência respiratória; irpm = incursões respiratórias por minuto; Sat O2 = saturação de oxigênio.
Figura 4: Algoritmo representando a triagem e o acolhimento de gestantes/parturientes nos diferentes serviços de saúde. (Adaptado de Poon et al. 202024.)
Cuidados intraparto
a) Os serviços de saúde devem designar uma área dentro da unidade para cuidar de gestantes com suspeita ou diagnóstico de COVID-19. Essa área deve ser restrita, com equipe diferente daquela que atende na área não COVID.
b) Na área não COVID, em decorrência do porcentual de assintomáticos e pré-sintomáticos que podem transmitir o vírus, recomenda-se que a equipe de saúde que realiza a assistência ao parto utilize equipamentos de proteção individual (EPIs), como máscara cirúrgica, protetor facial, gorro, avental e luvas em todos os partos.
c) Na área restrita (COVID), a equipe de saúde deve estar protegida, utilizando EPIs como máscara N95, protetor facial, gorro, avental e luvas. A máscara N95 é obrigatória durante procedimentos que produzem aerossóis, como expiração forçada durante a pressão, uso de oxigênio para reanimação intrauterina ou intubação.
d) Recomenda-se a redução de pessoas no momento do parto, mas a liberação de um acompanhante ficará a critério de cada serviço. Caso seja permitida a presença de um acompanhante, este deverá ser, obrigatoriamente, assintomático.
e) A via de parto deve obedecer às indicações obstétricas, ou seja, a infecção por SARS-CoV-2 não é indicação de cesárea, a menos que haja descompensação aguda da mãe e/ou do feto. Parturientes em insuficiência respiratória devem ser cuidadosamente avaliadas para decisão da resolução da gravidez, que, nesse caso, ocorrerá por cesárea.
f) Abreviar o segundo período do trabalho de parto com fórceps ou vácuo-extrator deve ser considerado, principalmente se a parturiente apresentar desconforto respiratório ou ocorrer sofrimento fetal agudo, respeitando-se as condições de aplicabilidade dos métodos.
g) Não há contraindicação para anestesia regional ou geral, mas o uso apropriado de EPI é incentivado.
h) Não há consenso na literatura sobre a ligadura precoce ou oportuna do cordão umbilical nem sobre o contato pele a pele, devendo cada serviço estabelecer seu protocolo assistencial e discutir com a parturiente a conduta preconizada no local.
Cuidados pós-parto
a) Em puérperas em boas condições recomenda-se a alta hospitalar precoce (24 horas para parto vaginal e 48 horas para cesárea). Isso limita a exposição da equipe de saúde e aumenta a disponibilidade do leito. A puérpera deverá completar 14 dias de isolamento domiciliar.
b) Recomenda-se manter o binômio mãe/recém-nascido no mesmo ambiente (quarto isolado), com a puérpera em uso de máscara e o berço do recém-nascido a dois metros do leito materno.
c) A amamentação é recomendada, a menos que a mãe esteja gravemente doente.
d) A equipe de saúde deve orientar a puérpera a praticar higiene respiratória, usar máscara cirúrgica, higienizar as mãos antes e depois de tocar no bebê e limpar e desinfetar as superfícies que tocou.
e) Se for usada extração de leite (ordenha), todo o equipamento deve ser limpo antes e após o uso.
f) A equipe de saúde que realiza a avaliação diária da evolução de puerpério deve utilizar EPIs.
g) Proibir visitas e restringir transportes intra e inter-hospitalares.
h) A presença de acompanhante no isolamento seguirá o protocolo assistencial de cada serviço.
i) As visitas pós-parto devem ser realizadas por telemedicina, a menos que a visita presencial seja essencial.
Transmissão vertical do SARS-CoV-2
Em relação à transmissão vertical do SARS-CoV-2, as evidências científicas são restritas a relatos de caso ou a revisões com pequeno número de casos e a maioria dos estudos não apontou transmissão vertical do vírus30-38. Em uma série de 9 gestantes com pneumonia por SARS-CoV-2, no terceiro trimestre de gestação, em Wuhan, a pesquisa para esse vírus em líquido amniótico, sangue do cordão umbilical e orofaringe dos recém-nascidos, além do leite materno, demonstrou resultado negativo, não evidenciando transmissão vertical para os recém-nascidos.30 Em outra série de casos de 38 gestantes, das quais 37 apresentavam RT-PCR positivo para SARS-CoV-2, com idade gestacional variando entre 30 semanas e 40 semanas, dentre os 30 recém-nascidos de mães com testes positivos nenhum neonato apresentou RT-PCR positivo para SARS-CoV-218.
Com o progredir da pandemia, novos dados foram publicados e foi com grande preocupação que a comunidade científica recebeu o relato de que recém-nascidos de mães com COVID-19 poderiam ter sido infectados por SARS-CoV-2 ainda intraútero. Numa coorte de 6 gestantes com RT-PCR positivo para COVID-19 e sintomas leves da doença foram realizadas dosagens de anticorpos específicos das classes IgG e IgM para SARS-CoV-2 no momento do nascimento, tanto nas mães como em seus filhos. Todos os neonatos nasceram de cesariana no terceiro trimestre, foram imediatamente isolados e submetidos a coleta de swabs nasofaríngeos para realizar RT-PCR. Todos os recém-nascidos apresentaram RT-PCR negativo para SARS-CoV-2 em swabs e em amostras de sangue. Os anticorpos IgG e IgM específicos para esse vírus foram detectados nos 6 neonatos, mas os anticorpos da classe M foram positivos em 2 neonatos. A detecção de anticorpos IgM específicos para SARS-CoV-2 em recém-nascidos poderia refletir a produção fetal após infecção intrauterina. No entanto, em nenhum recém-nascido houve isolamento viral por RT-PCR, portanto não há evidências virológicas de infecção congênita com transmissão intrauterina39. Vale também lembrar que a sensibilidade e a especificidade dos testes de IgM variam de acordo com a doença, mas geralmente são menos confiáveis que os testes moleculares. Recentemente a transmissão transplacentária de SARS-CoV-2 em um recém-nascido de mãe infectada no último trimestre foi demonstrada. A transmissão foi confirmada por um estudo virológico abrangente: a transmissão do SARS-CoV-2 causou inflamação placentária da viremia neonatal, demonstrada por exame histológico e imuno-histoquímica40. Nesse estudo, o neonato apresentou manifestação neurológica, consistente com as manifestações descritas em pacientes adultos infectados por esse vírus. A transmissão vertical do SARS-CoV-2, portanto, é possível, mas, felizmente, e ao contrário de outros vírus, sua capacidade de infectar o feto/recém-nascido parece ser pequena.
Como previamente citado, a COVID-19 tem se mostrado um grande desafio para a saúde pública mundial. O conhecimento sobre a fisiopatologia, o diagnóstico e o manejo melhora a cada dia, levando a mudança em condutas preconizadas. Como ginecologistas e obstetras, precisamos, diariamente, atualizar nossas informações para oferecer às mulheres, em uma das fases mais importantes de suas vidas, assistência obstétrica segura e de qualidade, sempre embasada em evidências científicas.
REFERÊNCIAS
- Gorbalenya AE, Baker SC, Baric RS, et al. Severe acute respiratory syndrome-related coronavirus: The species and its viruses – a statement of the Coronavirus Study Group. BioRxiv [Preprint]. [acessado em 18/2/2020]. Disponível em: https://www.biorxiv.org/content/10.1101/2020.02.07.937862v1. doi: https://doi.org/10.1101/2020.02.07.937862
- Ministério da Saúde do Brasil (MS). Painel Coronavírus. Abril de 2020 [acessado em 20/4/2020]. Disponível em: https://covid.saude.gov.br
- Ministério da Saúde do Brasil (MS). Protocolo de Manejo Clínico para o Novo Coronavírus (2019-nCoV) [acessado em 21/3/2020. Disponível em: https://portalarquivos2.saude.gov.br/images/pdf/2020/fevereiro/11/protocolo-manejo-coronavirus.pdf
- World Health Organization. (2020). Clinical management of severe acute respiratory infection when novel coronavirus (2019-nCoV) infection is suspected: interim guidance, 28 January 2020. World Health Organization. https://apps.who.int/iris/handle/10665/330893
- Protocolo de manejo dos casos suspeitos e confirmados para Infecção Humana pelo Novo Coronavírus (COVID-19) 24/03/2020. Versão 7 [acessado em 18/4/2020]. Disponível em: http://10.165.5.50/intranet/intranet.default.aspx
- Centers for Disease Control and Prevention (CDC). Interim Considerations for Infection Prevention and Control of Coronavirus Disease 2019 (COVID-19) in Inpatient Obstetric Healthcare Settings [acessado em 4/4/2020]. Disponível em: https://www.cdc.gov/coronavirus/2019-ncov/hcp/inpatient-obstetric-healthcare-guidance.html
- Ministério da Saúde do Brasil (MS). Boletim epidemiológico especial – COE COVID-19. Semana Epidemiológica 21 (17 a 23/05/2020). Disponível em: https://www.saude.gov.br/boletins-epidemiologicos
- Ferretti L, Wymant C, Kendall M, et al. Quantifying SARS-CoV-2 Transmission Suggests Epidemic Control With Digital Contact Tracing. Science. 2020 May 8;368(6491):eabb6936. doi: 10.1126/science.abb 6936. Epub 2020 Mar 31.
- Ministério da Saúde do Brasil (MS). Infecção Humana Pelo Novo Coronavírus (2019-nCoV). Boletim Epidemiológico COE 04/2020 [acessado em 31/3/2020]. Disponível em: https://www.saude.gov.br/boletins-epidemiologicos
- Secretaria de Estado da Saúde de São Paulo (SES). Diretrizes e orientações para funcionamento dos serviços de saúde para enfrentamento da pandemia do COVID-19 (novo coronavírus). Resolução SS-28, de 17/3/2020. DOE No 54, de 19/3/20, seção 1, p. 24. Disponível em: https://www.saopaulo.sp.gov.br/wp-content/uploads/2020/03/E_R-SS-CGOF-28_170320-1.pdf
- Chan JF-W, Yip CC-Y, To KK-W, et al. Improved molecular diagnosis of COVID19 by the novel, highly sensitive and specific COVID-19-RdRp/Hel real-time reverse transcription-PCR assay validated in vitro and with clinical specimens. J Clin Microbiol. 2020 Apr 23;58(5):e00310-20. doi: 10.1128/JCM.00310-20. Print 2020 Apr 23.
- World Health Organization (WHO). Laboratory testing for 2019 novel coronavirus (2019-nCoV) in suspected human cases. Interim guidance. January 17, 2020. WHO/nCoV/2020
- Lippi G, Simundic A-M, Plebani M. Potential preanalytical and analytical vulnerabilities in the laboratory diagnosis of coronavirus disease 2019 (COVID-19). Clin Chem Lab Med. 2020 Jun 25;58(7):1070-6. doi: 10.1515/cclm-2020-0285.
- Centers for Disease Control and Prevention (CDC). Severe Acute Respiratory Syndrome (SARS) and Coronavirus Testing—United States, 2003. MMWR Morb Mortal Wkly Rep. 2003 Apr 11;52(14):297-302.
- Tang Y-W, Schmitz JE, Persing DH, Stratton CW. Laboratory diagnosis of COVID-19: current issues and challenges. J Clin Microbiol. 2020 May 26;58(6):e00512-20. doi: 10.1128/JCM.00512-20. Print 2020 May 26.
- Chen N, Zhou M, Dong X, et al. Epidemiological and clinical characteristics of 99 cases of 2019 novel coronavirus pneumonia in Wuhan, China: a descriptive study. Lancet. 2020 Feb 15;395(10223):507-13. doi: 10.1016/S0140-6736(20)30211-7. Epub 2020 Jan 30.
- Siddiqi HK, Mehra MR. COVID-19 Illness in Native and Immunosuppressed States: A Clinical-Therapeutic Staging Proposal. J Heart Lung Transplant. 2020 May;39(5):405-7. doi: 10.1016/j.healun.2020.03.012. Epub 2020 Mar 20.
- Schwartz DA. An analysis of 38 pregnant women with COVID-19, their newborn infants, and maternal-fetal transmission of SARS-CoV-2: maternal coronavirus infections and pregnancy outcomes. Arch Pathol Lab Med. 2020 Mar 17. doi: 10.5858/arpa.2020-0901-SA. Online ahead of print.
- Mullins E, Evans D, Viner RM, O’Brien P, Morris E. Coronavirus in pregnancy and delivery: rapid review. Ultrasound Obstet Gynecol. 2020 May;55(5):586-92. doi: 10.1002/uog.22014.
- Di Mascio D, Khalil A, Saccone G, et al. Outcome of coronavirus spectrum infections (SARS, MERS, COVID-19) during pregnancy: a systematic review and meta-analysis. Am J Obstet Gynecol MFM. 2020 Mar 25;2(2):100107. doi: 10.1016/j.ajogmf.2020.100107. Online ahead of print.
- Rasmussen SA, Smulian JC, Lednicky JA, Wen TS, Jamieson DG. Coronavirus Disease 2019 (COVID-19) and pregnancy: What obstetricians need to know. Am J Obstet Gynecol. 2020 May;222(5):415-26. doi: 10.1016/j.ajog.2020.02.017. Epub 2020 Feb 24.
- The American College of Obstetricians and Gynecologists (ACOG). Novel Coronavirus 2019 (COVID-19). Practical advisory [acessado em 27/3/2020]. Disponível em: https://www.acog.org/clinical/clinical-guidance/practice-advisory/articles/2020/03/novel-coronavirus-2019
- Royal College of Obstetricians and Gynaecologists (RCOG). Coronavirus (COVID-19) Infection in Pregnancy. Version 10.1: Publicado em 19/6/2020 [acessado em 20/6/2020]. Disponível em: https://www.rcog.org.uk/globalassets/documents/guidelines/2020-06-18-coronavirus-covid-19-infection-in-pregnancy.pdf
- Poon LC, Yang H, Kapur A, et al. Global interim guidance on coronavirus disease 2019 (COVID‐19) during pregnancy and puerperium from FIGO and allied partners: Information for healthcare professionals. Int J Gynecol Obstet. April;149(3):273-86. doi: https://doi.org/10.1002/ijgo.13156
- Duarte G, Quintana SM. Infecção pelo Coronavírus SARS-CoV-2 em Obstetrícia. Enfrentando o desconhecido! Portal SOGESP. Publicado em 21/3/2020. Disponível em: https://www.sogesp.com.br/noticias/infeccao-pelo-coronavirus-sars-cov-2-em-obstetricia-enfrentando-o-desconhecido/
- Osanan GC, Bonomi IBA, Bacha CA, Laranjeira CLS, Ramos Filho FL, Aguiar RALP. Coronavirus na gravidez: considerações e recomendações SOGIMIG. Portal SOGIMIG. Publicado em 20/3/2020. Disponível em: http://www.sogimig.org.br/wp-content/uploads/2020/03/Sogimig-Orientações-sobre-Covid-19-1.pdf
- Narang K, Ibirogba ER, Elrefaei A, et al. SARS-CoV-2 in Pregnancy: A Comprehensive Summary of Current Guidelines. J Clin Med. 2020 May 18;9(5):1521. doi: 10.3390/jcm9051521
- Mazzoni AAS, Almado CEL, Nicolini EA, et al. Protocolo de manejo dos casos graves confirmados de infecção pelo novo coronavírus (COVID-19) tratados na UTI COVID. Hospital das Clínicas da FMRPUSP. Versão 5. Publicado em 11/6/2020. Disponível em: https://site.hcrp.usp.br/covid/saude-protocolo-manejo-suspeitos.php
- World Health Organization (WHO). Clinical management of severe acute respiratory infection (SARI) when COVID-19 disease is suspected: interim guidance, 13 March 2020. World Health Organization. Disponível em: https://apps.who.int/iris/handle/10665/331446.
- Chen H, Guo J, Wang C, et al. Clinical characteristics and intrauterine vertical transmission potential of COVID-19 infection in nine pregnant women: a retrospective review of medical records. Lancet. 2020 Mar 7;395(10226):809-15. doi: 10.1016/S0140-6736(20)30360-3. Epub 2020 Feb 12.
- Zhu H, Wang L, Fang C, et al. Clinical analysis of 10 neonates born to mothers with 2019-nCoV pneumonia. Transl Pediatr. 2020 Feb;9(1):51-60. doi: 10.21037/tp.2020.02.06
- Liu W, Zhang Q, Chen J, et al. Detection of Covid-19 in Children in Early January 2020 in Wuhan, China. N Engl J Med. 2020 Apr 2;382(14):1370-1. doi: 10.1056/NEJMc2003717. Epub 2020 Mar 12
- Zeng L, Xia S, Yuan W, et al. Neonatal Early-Onset Infection With SARS-CoV-2 in 33 Neonates Born to Mothers With COVID-19 in Wuhan, China. JAMA Pediatr. 2020 Mar 26;e200878. doi: 10.1001/jamapediatrics.2020.0878. Online ahead of print.
- Wang L, Shi Y, Xiao T, et al. Chinese expert consensus on the perinatal and neonatal management for the prevention and control of the 2019 novel coronavirus infection (First edition). Ann Transl Med. 2020 Feb;8(3):47. doi: 10.21037/atm.2020.02.20
- Elshafeey F, Magdi R, Hindi N, et al. A Systematic Scoping Review of COVID-19 During Pregnancy and Childbirth. Int J Gynaecol Obstet. 2020 Jul;150(1):47-52. doi: 10.1002/ijgo.13182. Epub 2020 May 17.
- Yang L, Ruihong Z, Zheng S, et al. Lack of Vertical Transmission of Severe Acute Respiratory Syndrome Coronavirus 2, China. Emerg Infect Dis. 2020 Jun;26(6):1335-6. doi: 10.3201/eid2606.200287. Epub 2020 Jun 17.
- Lu D, Sang L, Du S, Li T, Chang Y, Yang X-A. Asymptomatic COVID-19 Infection in Late Pregnancy Indicated No Vertical Transmission. J Med Virol. 2020 Apr 24;10.1002/jmv.25927. doi: 10.1002/jmv.25927. Online ahead of print.
- Alzamora MC, Paredes T, Caceres D, Webb CM, Valdez LM, La Rosa M. Severe COVID-19 During Pregnancy and Possible Vertical Transmission. Am J Perinatol. 2020 Apr 18. doi: 10.1055/s-0040-1710050. Online ahead of print.
- Zeng H, Xu C, Fan J, et al. Antibodies in infants born to mothers with COVID-19 pneumonia. JAMA. 2020 Mar 26;323(18):1848-9. doi: 10.1001/jama.2020.4861. Online ahead of print.
- Vivanti A, Vauloup-Fellous C, Prevot S, et al. Transplacental transmission of SARS-CoV-2 infection. Maternal & Fetal Medicine. doi: 10.21203/rs.3.rs-28884/v1. Posted 15 May, 2020. Under review.
Microsoft.CSharp.RuntimeBinder.RuntimeBinderException: 'Newtonsoft.Json.Linq.JValue' does not contain a definition for 'macroAlias' at CallSite.Target(Closure , CallSite , Object ) at System.Dynamic.UpdateDelegates.UpdateAndExecute1[T0,TRet](CallSite site, T0 arg0) at CallSite.Target(Closure , CallSite , Object ) at AspNetCore.Views_Partials_grid_editors_macro.ExecuteAsync() in C:\Domains\sogesp.com.br\www\Views\Partials\grid\editors\macro.cshtml:line 0 at Microsoft.AspNetCore.Mvc.Razor.RazorView.RenderPageCoreAsync(IRazorPage page, ViewContext context) at Microsoft.AspNetCore.Mvc.Razor.RazorView.RenderPageAsync(IRazorPage page, ViewContext context, Boolean invokeViewStarts) at Microsoft.AspNetCore.Mvc.Razor.RazorView.RenderAsync(ViewContext context) at Microsoft.AspNetCore.Mvc.ViewFeatures.HtmlHelper.RenderPartialCoreAsync(String partialViewName, Object model, ViewDataDictionary viewData, TextWriter writer) at Microsoft.AspNetCore.Mvc.ViewFeatures.HtmlHelper.PartialAsync(String partialViewName, Object model, ViewDataDictionary viewData) at AspNetCore.Views_Partials_grid_editors_base.ExecuteAsync() in C:\Domains\sogesp.com.br\www\Views\Partials\grid\editors\base.cshtml:line 11
 11 99167-0001
11 99167-0001  11 3884-7100
11 3884-7100 
